西安辦理第二類(lèi)醫(yī)療器械產(chǎn)品注冊(cè)證及銷(xiāo)售企業(yè)申請(qǐng)條件詳解
在西安從事第二類(lèi)醫(yī)療器械的生產(chǎn)與銷(xiāo)售,企業(yè)必須嚴(yán)格遵守國(guó)家及地方相關(guān)法規(guī),分別獲取《醫(yī)療器械注冊(cè)證》和《醫(yī)療器械經(jīng)營(yíng)許可證》。以下是針對(duì)在西安辦理第二類(lèi)醫(yī)療器械產(chǎn)品注冊(cè)證以及從事銷(xiāo)售活動(dòng)的企業(yè)所需滿(mǎn)足的核心申請(qǐng)條件的詳細(xì)說(shuō)明。
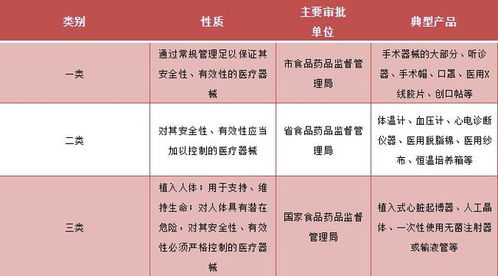
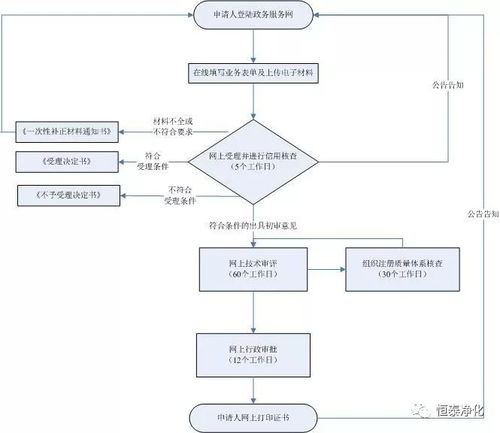
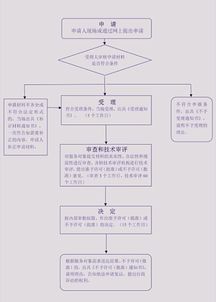
一、 第二類(lèi)醫(yī)療器械產(chǎn)品注冊(cè)證申請(qǐng)條件
產(chǎn)品注冊(cè)證是針對(duì)醫(yī)療器械產(chǎn)品本身的上市許可,由生產(chǎn)企業(yè)或注冊(cè)申請(qǐng)人(如總代)向陜西省藥品監(jiān)督管理局提出申請(qǐng)。主要條件包括:
- 申請(qǐng)主體資格:申請(qǐng)人應(yīng)為在中華人民共和國(guó)境內(nèi)依法登記的企業(yè),能夠獨(dú)立承擔(dān)法律責(zé)任。境外申請(qǐng)人需指定中國(guó)境內(nèi)的企業(yè)法人作為代理人。
- 質(zhì)量管理體系:申請(qǐng)人必須建立符合《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》(GMP)要求的質(zhì)量管理體系,并在申請(qǐng)注冊(cè)前或向省藥監(jiān)局提交體系核查申請(qǐng),接受現(xiàn)場(chǎng)檢查。對(duì)于注冊(cè)人制度下的委托生產(chǎn),委托方和受托生產(chǎn)企業(yè)均需具備相應(yīng)的質(zhì)量管理能力。
- 產(chǎn)品技術(shù)要求:產(chǎn)品必須已研制完成,其安全性、有效性得到科學(xué)驗(yàn)證。申請(qǐng)人需提交詳盡的產(chǎn)品技術(shù)要求、風(fēng)險(xiǎn)分析報(bào)告、產(chǎn)品檢驗(yàn)報(bào)告(需由具有資質(zhì)的醫(yī)療器械檢驗(yàn)機(jī)構(gòu)出具)、臨床評(píng)價(jià)資料(通常為同品種比對(duì)或臨床試驗(yàn)報(bào)告)等全套技術(shù)資料。
- 產(chǎn)品檢驗(yàn)報(bào)告:產(chǎn)品必須通過(guò)具有資質(zhì)的醫(yī)療器械檢驗(yàn)機(jī)構(gòu)的型式檢驗(yàn),并出具合格的檢驗(yàn)報(bào)告。
- 說(shuō)明書(shū)與標(biāo)簽:擬定的產(chǎn)品說(shuō)明書(shū)和標(biāo)簽應(yīng)符合《醫(yī)療器械說(shuō)明書(shū)和標(biāo)簽管理規(guī)定》的要求。
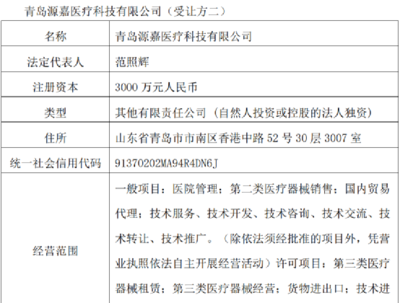
二、 第二類(lèi)醫(yī)療器械銷(xiāo)售(經(jīng)營(yíng))企業(yè)申請(qǐng)條件
銷(xiāo)售企業(yè)需向經(jīng)營(yíng)場(chǎng)所所在地的市級(jí)市場(chǎng)監(jiān)督管理局(西安市市場(chǎng)監(jiān)督管理局)申請(qǐng)《第二類(lèi)醫(yī)療器械經(jīng)營(yíng)備案憑證》(注意:經(jīng)營(yíng)第二類(lèi)醫(yī)療器械實(shí)行備案制,而非許可制,但仍需滿(mǎn)足條件并獲取憑證)。主要條件包括:
- 企業(yè)資質(zhì):企業(yè)應(yīng)具有與經(jīng)營(yíng)范圍和規(guī)模相適應(yīng)的企業(yè)法人或非法人企業(yè)資格。
- 經(jīng)營(yíng)場(chǎng)所與倉(cāng)儲(chǔ)條件:
- 擁有與經(jīng)營(yíng)規(guī)模和品種相適應(yīng)的固定經(jīng)營(yíng)場(chǎng)所和庫(kù)房。經(jīng)營(yíng)場(chǎng)所和庫(kù)房不得設(shè)在居民住宅內(nèi)。
- 經(jīng)營(yíng)場(chǎng)所和庫(kù)房的面積、布局、環(huán)境(如溫濕度控制、避光、防塵等)應(yīng)能滿(mǎn)足所經(jīng)營(yíng)醫(yī)療器械的儲(chǔ)存、展示要求。若經(jīng)營(yíng)有特殊儲(chǔ)存要求的產(chǎn)品(如體外診斷試劑),需配備冷庫(kù)等設(shè)施。
- 質(zhì)量管理人員:企業(yè)負(fù)責(zé)人應(yīng)熟悉醫(yī)療器械相關(guān)法規(guī)。必須配備與經(jīng)營(yíng)規(guī)模相適應(yīng)的質(zhì)量管理人員,如質(zhì)量負(fù)責(zé)人。質(zhì)量負(fù)責(zé)人應(yīng)具備醫(yī)療器械相關(guān)專(zhuān)業(yè)(如醫(yī)學(xué)、藥學(xué)、生物工程等)大專(zhuān)以上學(xué)歷或中級(jí)以上職稱(chēng),并具有3年以上醫(yī)療器械經(jīng)營(yíng)質(zhì)量管理工作經(jīng)驗(yàn)。
- 質(zhì)量管理制度:企業(yè)應(yīng)建立覆蓋采購(gòu)、驗(yàn)收、儲(chǔ)存、銷(xiāo)售、運(yùn)輸、售后服務(wù)等環(huán)節(jié)的完善的質(zhì)量管理制度,包括質(zhì)量管理職責(zé)、采購(gòu)與收貨、驗(yàn)收、儲(chǔ)存與養(yǎng)護(hù)、銷(xiāo)售與出庫(kù)、運(yùn)輸與售后服務(wù)、不合格品處理、追溯管理、不良事件監(jiān)測(cè)和報(bào)告等。
- 計(jì)算機(jī)信息管理系統(tǒng):鼓勵(lì)或要求企業(yè)使用符合醫(yī)療器械經(jīng)營(yíng)質(zhì)量管理要求的計(jì)算機(jī)信息管理系統(tǒng),實(shí)現(xiàn)對(duì)經(jīng)營(yíng)全過(guò)程的可追溯管理。
- 售后服務(wù)能力:應(yīng)具備對(duì)其所銷(xiāo)售產(chǎn)品提供售后服務(wù)、技術(shù)培訓(xùn)以及協(xié)助處理不良事件的能力。
與流程要點(diǎn)
- 分開(kāi)辦理:“產(chǎn)品注冊(cè)”與“經(jīng)營(yíng)備案”是兩個(gè)獨(dú)立的監(jiān)管環(huán)節(jié)。生產(chǎn)或代理產(chǎn)品需先取得產(chǎn)品注冊(cè)證;想要銷(xiāo)售該產(chǎn)品,企業(yè)自身還需辦理經(jīng)營(yíng)備案。
- 核心區(qū)別:注冊(cè)證關(guān)乎產(chǎn)品本身的安全有效,審查重點(diǎn)是技術(shù)資料和質(zhì)量管理體系;經(jīng)營(yíng)備案關(guān)乎銷(xiāo)售企業(yè)的規(guī)范運(yùn)營(yíng)能力,審查重點(diǎn)是場(chǎng)地、人員、制度等經(jīng)營(yíng)條件。
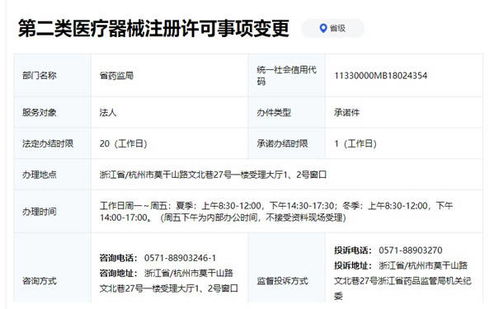
- 辦理部門(mén):產(chǎn)品注冊(cè)向陜西省藥品監(jiān)督管理局申報(bào);經(jīng)營(yíng)備案向西安市市場(chǎng)監(jiān)督管理局(或其指定的區(qū)級(jí)局)提交備案材料。
- 動(dòng)態(tài)合規(guī):取得資質(zhì)后,企業(yè)需持續(xù)遵守法規(guī),接受監(jiān)管部門(mén)的監(jiān)督檢查,并履行產(chǎn)品追溯、不良事件監(jiān)測(cè)等義務(wù)。
建議企業(yè)在正式申請(qǐng)前,詳細(xì)查閱國(guó)家藥品監(jiān)督管理局及陜西省、西安市藥監(jiān)局發(fā)布的最新法規(guī)文件,或咨詢(xún)專(zhuān)業(yè)服務(wù)機(jī)構(gòu),以確保完全符合所有現(xiàn)行要求。
如若轉(zhuǎn)載,請(qǐng)注明出處:http://www.baidu0951.com/product/16.html
更新時(shí)間:2026-05-11 07:39:32