政策東風加速創(chuàng)新藥械落地 從“港澳藥械通”看第一類醫(yī)療器械的市場機遇
我國醫(yī)藥健康領域改革步伐不斷加快,一系列旨在優(yōu)化審評審批、加速創(chuàng)新產(chǎn)品上市的政策相繼出臺。其中,“真實世界數(shù)據(jù)”的應用與“港澳藥械通”等政策的落地,正為醫(yī)療器械,尤其是第一類醫(yī)療器械的研發(fā)、獲批與銷售,注入強勁動力,開啟了行業(yè)發(fā)展的新篇章。
政策組合拳:疏通藥械上市“快車道”
1. 真實世界數(shù)據(jù)(RWD)的價值釋放
傳統(tǒng)醫(yī)療器械的臨床試驗往往周期長、成本高。而“真實世界數(shù)據(jù)”指在日常醫(yī)療實踐中收集的與患者健康狀況和/或診療及保健有關的數(shù)據(jù)。國家藥監(jiān)局已發(fā)布相關指導原則,鼓勵將真實世界證據(jù)用于支持醫(yī)療器械的臨床評價。對于部分第一類醫(yī)療器械(風險程度低,實行常規(guī)管理即可保證其安全、有效)而言,利用在臨床使用中積累的真實世界數(shù)據(jù)來證明其安全有效性,可以簡化臨床評價要求,顯著縮短產(chǎn)品上市前的驗證周期,降低企業(yè)成本,使產(chǎn)品能更快地服務于臨床需求。
2. “港澳藥械通”政策的橋梁作用
“港澳藥械通”政策允許在粵港澳大灣區(qū)內(nèi)地指定的醫(yī)療機構,使用已在香港、澳門上市但未在內(nèi)地注冊的臨床急需藥品和醫(yī)療器械。這一政策具有雙重加速效應:
- 先行先試,積累數(shù)據(jù):國際先進的醫(yī)療器械可率先在指定醫(yī)療機構使用,其產(chǎn)生的臨床使用數(shù)據(jù)和經(jīng)驗,可以作為該產(chǎn)品未來正式申請在內(nèi)地上市的重要參考和證據(jù),特別是寶貴的真實世界數(shù)據(jù)。
- 市場預熱與渠道探索:對于有意進入內(nèi)地市場的境外第一類醫(yī)療器械,該政策提供了一個低風險的市場切入點和渠道試水機會。通過早期在高端醫(yī)療機構的臨床應用,可以建立品牌認知度,了解內(nèi)地市場的實際需求與操作流程,為后續(xù)大規(guī)模市場推廣鋪平道路。
聚焦第一類醫(yī)療器械:在簡政放權中抓住銷售先機
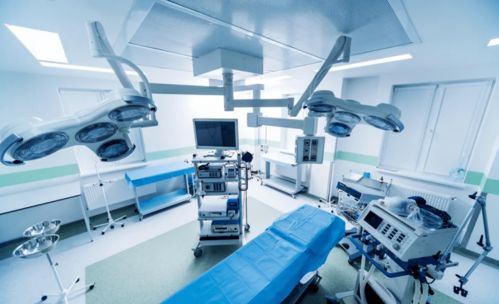
第一類醫(yī)療器械通常包括外科用器械、病房護理設備、部分物理治療設備等基礎型、低風險產(chǎn)品。在現(xiàn)行法規(guī)下,其備案管理流程已相對簡化。而上述宏觀政策的推進,進一步為其市場拓展創(chuàng)造了有利條件:
1. 上市路徑更便捷:企業(yè)可以更靈活地運用真實世界證據(jù)支持備案,加速產(chǎn)品完成上市前合規(guī)步驟。對于已有港澳上市記錄的產(chǎn)品,通過“藥械通”通道積累的內(nèi)地使用經(jīng)驗,能進一步增強其安全有效性說服力,簡化注冊備案材料。
2. 市場準入效率提升:政策整體營造了鼓勵創(chuàng)新、快速響應的監(jiān)管環(huán)境。醫(yī)療機構,尤其是大灣區(qū)內(nèi)的機構,對新器械、新技術的接受度和試用意愿可能因政策引導而提高。這為第一類醫(yī)療器械的臨床推廣和銷售提供了更友好的早期環(huán)境。
3. 銷售策略的聯(lián)動與創(chuàng)新:銷售企業(yè)可以關注通過“港澳藥械通”進入內(nèi)地機構的器械名單,這些產(chǎn)品往往代表了一定的技術先進性和市場潛力。可以前瞻性地與相關生產(chǎn)企業(yè)建立聯(lián)系,布局未來代理或銷售合作。利用政策帶來的市場關注度,加強自身對第一類器械的學術推廣和專業(yè)服務能力,從單純的渠道商向解決方案提供商轉(zhuǎn)型。
展望與建議
“真實世界數(shù)據(jù)”應用與“港澳藥械通”等政策,是深化醫(yī)藥衛(wèi)生體制改革、滿足人民群眾健康需求的重要舉措。它們不僅加速了高端創(chuàng)新藥械的可及性,也為整個醫(yī)療器械產(chǎn)業(yè)鏈,包括看似“普通”的第一類醫(yī)療器械,帶來了結構性的機遇。
對于醫(yī)療器械生產(chǎn)企業(yè)及銷售商而言,應當:
- 深入研究政策細節(jié),主動學習利用真實世界研究支持產(chǎn)品評價的方法。
- 關注粵港澳大灣區(qū)的動態(tài),探索利用“藥械通”等渠道進行產(chǎn)品先行布局的可能性。
- 強化產(chǎn)品全生命周期質(zhì)量管理,即使對于備案管理的第一類器械,也需確保安全有效,積累良好數(shù)據(jù)與口碑。
- 創(chuàng)新商業(yè)模式,結合政策導向和臨床實際需求,提供更具價值的產(chǎn)品與服務組合。
在政策東風的吹拂下,中國醫(yī)療器械市場正迎來一個更加開放、高效、以臨床價值為導向的新階段。準確把握政策脈搏,順勢而為,將是企業(yè)在競爭中脫穎而出的關鍵。
如若轉(zhuǎn)載,請注明出處:http://www.baidu0951.com/product/24.html
更新時間:2026-05-11 22:05:53