浙江省第二類醫(yī)療器械注冊(cè)變更資料要求與第一類醫(yī)療器械銷售規(guī)范解析
在醫(yī)療器械行業(yè)的合規(guī)經(jīng)營中,企業(yè)不僅需要關(guān)注產(chǎn)品的注冊(cè)準(zhǔn)入,還需對(duì)已獲證產(chǎn)品的變更管理以及不同類別產(chǎn)品的銷售活動(dòng)有清晰的認(rèn)識(shí)。本文將聚焦于浙江省第二類醫(yī)療器械的注冊(cè)變更資料要求,并簡(jiǎn)述第一類醫(yī)療器械的銷售相關(guān)規(guī)范,為相關(guān)從業(yè)者提供參考。
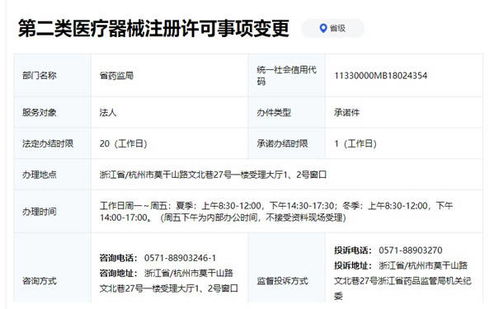
一、 浙江省第二類醫(yī)療器械注冊(cè)變更資料要求
根據(jù)國家藥品監(jiān)督管理局(NMPA)發(fā)布的《醫(yī)療器械注冊(cè)與備案管理辦法》及相關(guān)配套文件,并結(jié)合浙江省藥品監(jiān)督管理局的具體執(zhí)行要求,第二類醫(yī)療器械注冊(cè)證持有者在產(chǎn)品注冊(cè)證有效期內(nèi),若發(fā)生需要變更的事項(xiàng),必須向原注冊(cè)部門(浙江省藥監(jiān)局)提交變更申請(qǐng)。變更類型主要分為登記事項(xiàng)變更和許可事項(xiàng)變更。
1. 變更類型區(qū)分
- 登記事項(xiàng)變更:指注冊(cè)人名稱和住所、代理人名稱和住所等事項(xiàng)的變更。此類變更相對(duì)簡(jiǎn)易。
- 許可事項(xiàng)變更:指產(chǎn)品名稱、型號(hào)、規(guī)格、結(jié)構(gòu)及組成、適用范圍、產(chǎn)品技術(shù)要求、進(jìn)口醫(yī)療器械的生產(chǎn)地址等可能影響產(chǎn)品安全性、有效性的實(shí)質(zhì)性變更。此類變更要求嚴(yán)格,通常需要提交詳實(shí)的技術(shù)資料。
2. 通用資料要求核心清單
無論何種變更,申請(qǐng)人均需提交基礎(chǔ)性文件,但根據(jù)變更內(nèi)容的不同,技術(shù)性資料的深度和廣度差異顯著。核心通用資料通常包括:
- 醫(yī)療器械注冊(cè)變更申請(qǐng)表。
- 證明性文件:如企業(yè)營業(yè)執(zhí)照副本、原醫(yī)療器械注冊(cè)證及其附件復(fù)印件。
- 注冊(cè)人關(guān)于變更情況的聲明,承諾變更內(nèi)容真實(shí)、合法。
- 關(guān)于變更情況相關(guān)的說明材料。
3. 許可事項(xiàng)變更的技術(shù)資料重點(diǎn)
對(duì)于涉及產(chǎn)品技術(shù)本身的許可事項(xiàng)變更,是資料準(zhǔn)備的核心與難點(diǎn),可能要求提交:
- 變化情況對(duì)比表及說明:詳細(xì)列明變更前后所有技術(shù)內(nèi)容、性能指標(biāo)、臨床評(píng)價(jià)資料等的變化,并闡述變化原因及依據(jù)。
- 修訂后的產(chǎn)品技術(shù)要求:完整版本,并標(biāo)注所有變更處。
- 針對(duì)變化部分的研究資料:包括但不限于設(shè)計(jì)驗(yàn)證、工藝驗(yàn)證、風(fēng)險(xiǎn)分析更新、生物相容性評(píng)價(jià)(若涉及)、滅菌驗(yàn)證(若涉及)、穩(wěn)定性研究等。變更可能對(duì)產(chǎn)品安全性、有效性產(chǎn)生影響的,需提供充分證據(jù)。
- 臨床評(píng)價(jià)資料:如果變更可能影響產(chǎn)品的臨床使用安全性或有效性,可能需要通過臨床試驗(yàn)、同品種對(duì)比或臨床文獻(xiàn)數(shù)據(jù)等方式,補(bǔ)充或更新臨床評(píng)價(jià)資料。
- 產(chǎn)品檢驗(yàn)報(bào)告:通常需要提供具有醫(yī)療器械檢驗(yàn)資質(zhì)的機(jī)構(gòu)出具的、符合修訂后產(chǎn)品技術(shù)要求的注冊(cè)檢驗(yàn)報(bào)告。
- 符合性聲明:聲明變更后的產(chǎn)品符合現(xiàn)行法規(guī)及強(qiáng)制性標(biāo)準(zhǔn)的要求。
4. 浙江省地方性要求提示
企業(yè)應(yīng)密切關(guān)注浙江省藥監(jiān)局官方網(wǎng)站發(fā)布的辦事指南、通知公告,了解最新的表格格式、電子申報(bào)系統(tǒng)使用要求、紙質(zhì)材料遞交方式等具體流程細(xì)節(jié)。建議在準(zhǔn)備資料前,與省局相關(guān)受理或技術(shù)審評(píng)部門進(jìn)行預(yù)先溝通。
二、 第一類醫(yī)療器械銷售規(guī)范簡(jiǎn)述
與第二類醫(yī)療器械的注冊(cè)管理不同,第一類醫(yī)療器械實(shí)行產(chǎn)品備案管理。其生產(chǎn)活動(dòng)由設(shè)區(qū)的市級(jí)藥品監(jiān)督管理部門備案,而銷售活動(dòng)的監(jiān)管重點(diǎn)在于經(jīng)營行為的合規(guī)性。
1. 經(jīng)營資質(zhì)要求
- 從事第一類醫(yī)療器械銷售的企業(yè),無需辦理《醫(yī)療器械經(jīng)營許可證》。
- 但經(jīng)營者應(yīng)當(dāng)具備與其經(jīng)營規(guī)模和范圍相適應(yīng)的經(jīng)營場(chǎng)所和貯存條件,以及相應(yīng)的質(zhì)量管理制度和專業(yè)人員。
- 根據(jù)《醫(yī)療器械經(jīng)營監(jiān)督管理辦法》,從事醫(yī)療器械批發(fā)業(yè)務(wù)的企業(yè),其銷售對(duì)象必須是具備合法資質(zhì)的醫(yī)療器械生產(chǎn)經(jīng)營企業(yè)或使用單位。
2. 合規(guī)銷售要點(diǎn)
- 產(chǎn)品合法性:確保所銷售的第一類醫(yī)療器械已取得有效的醫(yī)療器械備案憑證,產(chǎn)品標(biāo)簽、說明書內(nèi)容與備案信息一致。
- 進(jìn)貨查驗(yàn)記錄:必須建立并執(zhí)行進(jìn)貨查驗(yàn)記錄制度,記錄內(nèi)容包括產(chǎn)品名稱、型號(hào)、規(guī)格、生產(chǎn)批號(hào)、有效期、備案人/生產(chǎn)企業(yè)名稱、供貨者名稱及聯(lián)系方式、進(jìn)貨數(shù)量、進(jìn)貨日期等。相關(guān)記錄和憑證需保存至產(chǎn)品有效期后2年,且不少于5年。
- 銷售記錄:特別是從事批發(fā)業(yè)務(wù)的企業(yè),應(yīng)建立銷售記錄制度,確保產(chǎn)品可追溯。
- 廣告宣傳:醫(yī)療器械廣告內(nèi)容必須真實(shí)、合法,以藥品監(jiān)督管理部門批準(zhǔn)的注冊(cè)/備案證明文件為準(zhǔn),不得含有虛假、夸大內(nèi)容。
- 網(wǎng)絡(luò)銷售:若通過網(wǎng)絡(luò)銷售第一類醫(yī)療器械,應(yīng)依法向所在地設(shè)區(qū)的市級(jí)藥品監(jiān)督管理部門辦理經(jīng)營備案,并在其主頁面顯著位置展示其醫(yī)療器械經(jīng)營備案憑證等信息。
三、
對(duì)于浙江省的醫(yī)療器械企業(yè)而言,第二類醫(yī)療器械的注冊(cè)變更是一項(xiàng)嚴(yán)肅的技術(shù)評(píng)審過程,要求企業(yè)系統(tǒng)、嚴(yán)謹(jǐn)?shù)販?zhǔn)備資料,尤其是證明變更不影響安全有效的核心技術(shù)文件。而對(duì)于第一類醫(yī)療器械的銷售,雖然準(zhǔn)入門檻較低,但事中事后的合規(guī)經(jīng)營責(zé)任同樣重大,企業(yè)需建立健全質(zhì)量管理體系,確保產(chǎn)品來源清、去向明,合法合規(guī)開展銷售活動(dòng)。兩者共同構(gòu)成了醫(yī)療器械全生命周期管理的重要環(huán)節(jié),是企業(yè)穩(wěn)健發(fā)展的基石。
如若轉(zhuǎn)載,請(qǐng)注明出處:http://www.baidu0951.com/product/23.html
更新時(shí)間:2026-05-11 12:40:30