深入理解《醫療器械產品出口銷售證明管理規定》 聚焦第一類醫療器械的出口銷售實務

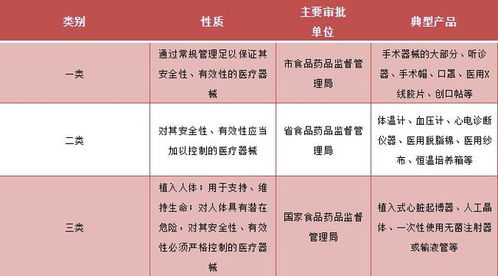
《醫療器械產品出口銷售證明管理規定》(以下簡稱《規定》)是規范我國醫療器械出口活動、保障產品質量與國際信譽的重要法規文件。對于從事第一類醫療器械(通常為風險程度低,實行常規管理可以保證其安全、有效的醫療器械,如部分外科器械、病床等)出口銷售的企業而言,深入學習并準確理解該《規定》具有至關重要的現實意義。
一、 核心目的與適用范圍
《規定》的核心目的是確保擬出口的醫療器械產品符合我國及進口國(地區)的相關要求,維護“中國制造”醫療器械的國際聲譽。它明確適用于所有在中國境內已取得醫療器械產品注冊/備案,并擬向境外出口的醫療器械。對于第一類醫療器械而言,由于其在國內實行備案管理(而非注冊),企業在申請出口銷售證明時,必須確保該產品已完成第一類醫療器械產品備案,并取得合法有效的備案憑證。這是申請出口證明的前提和基礎。
二、 申請條件與核心要求(針對第一類醫療器械)
1. 備案有效性:出口企業必須是該第一類醫療器械的備案人,或已獲得備案人的合法授權。產品備案信息(如型號規格、預期用途等)必須真實、準確、有效,且備案狀態為“有效”。
2. 質量體系要求:盡管第一類醫療器械生產備案要求相對簡化,但生產企業仍需建立符合《醫療器械生產質量管理規范》基本要求的質量管理體系,保證產品持續符合強制性標準及備案的產品技術要求。出口企業應能提供相關的符合性聲明或證據。
3. 產品合規性:出口產品必須符合中國現行的強制性國家標準或行業標準。如果目標市場有特定法規或標準要求(如CE認證、FDA注冊等),企業應自行確保產品符合,但這通常不屬于我國出具《醫療器械產品出口銷售證明》的直接審查內容。證明文件主要證明該產品在中國境內的合法身份。
三、 證明文件的性質與作用
《醫療器械產品出口銷售證明》是一份官方證明文件,而非貿易許可或質量認證。它主要用于:
向進口國監管機構證明,該醫療器械已在中國境內獲得合法的上市資格(備案)。
供中國海關辦理出口通關手續時使用。
* 作為國際貿易中,證明產品來源及合規基礎的重要支持性文件。
對于進口商或國外監管機構而言,這份證明是驗證產品中國源頭合法性的關鍵依據之一。
四、 對第一類醫療器械出口企業的實踐啟示
1. 備案先行,確保源頭合法:在開展出口業務前,務必完成第一類醫療器械產品備案和生產備案(如涉及生產),并確保所有備案信息與出口產品完全一致。
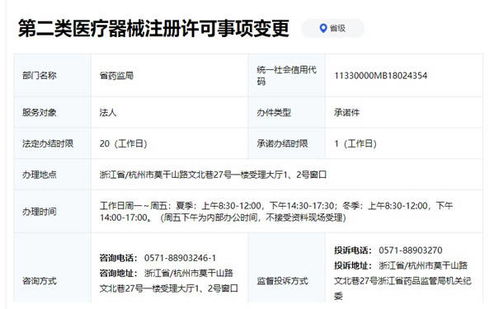
2. 動態管理,及時更新:關注備案信息的有效性。若產品備案信息發生變更,需及時辦理備案變更手續,確保出口證明申請依據的備案信息始終處于最新有效狀態。
3. 理解差異,雙重合規:深刻認識到中國備案與目標市場準入要求的差異。取得中國的出口銷售證明,不代表自動滿足進口國要求。企業需主動研究并滿足目標市場的法規,如是否需要CE標志、FDA列名等,實現“雙重合規”。
4. 保留記錄,應對核查:建立健全的出口產品檔案,包括備案憑證、質量標準、檢測報告、購銷合同、出口證明副本等,以備國內外監管部門的監督檢查。
**
對《醫療器械產品出口銷售證明管理規定》的學習,對于第一類醫療器械出口企業而言,重點在于厘清 “國內備案”與“出口證明”之間的關系,明確出口證明的證明屬性而非許可屬性,并牢固樹立起從源頭備案到最終出口的全流程合規意識**。只有將《規定》的要求內化于日常經營管理中,才能確保出口業務順暢、穩健,在全球市場上樹立負責任的中國醫療器械供應商形象。
如若轉載,請注明出處:http://www.baidu0951.com/product/11.html
更新時間:2026-05-11 21:30:15