第二類醫(yī)療器械銷售全攻略 從注冊到市場準入的關(guān)鍵步驟解析

引言:第二類醫(yī)療器械的重要性
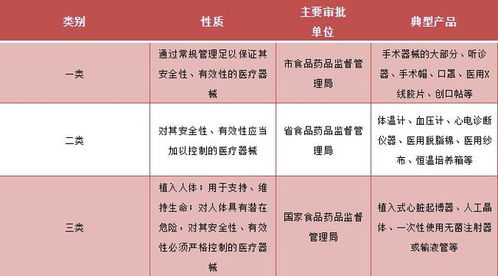
第二類醫(yī)療器械在醫(yī)療健康領(lǐng)域中扮演著至關(guān)重要的角色。它們通常具有中度風(fēng)險,需要嚴格控制管理以保證其安全性和有效性,例如血壓計、心電圖機、超聲診斷設(shè)備、部分手術(shù)器械、醫(yī)用敷料等。成功完成第二類醫(yī)療器械的注冊并實現(xiàn)合規(guī)銷售,是進入市場、服務(wù)患者、實現(xiàn)商業(yè)價值的前提。本文將系統(tǒng)梳理第二類醫(yī)療器械從注冊到銷售的全流程核心事項。
第一部分:第二類醫(yī)療器械注冊核心流程
1. 注冊前的準備與分類判定
* 首要步驟:準確分類。 企業(yè)需根據(jù)國家藥品監(jiān)督管理局發(fā)布的《醫(yī)療器械分類目錄》,結(jié)合產(chǎn)品的預(yù)期用途、結(jié)構(gòu)特征、使用方式等,判定產(chǎn)品是否確實屬于第二類醫(yī)療器械。分類是后續(xù)所有工作的基礎(chǔ),分類錯誤將導(dǎo)致整個注冊路徑錯誤。
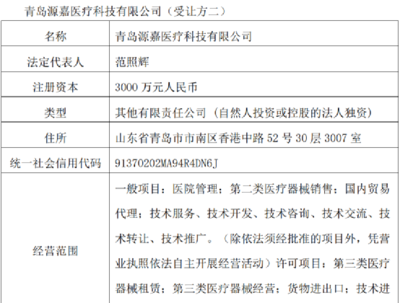
- 主體資格確認。 注冊申請人必須是依法在中國境內(nèi)設(shè)立的企業(yè)(包括研發(fā)和生產(chǎn)機構(gòu)),并具備與所申請產(chǎn)品相適應(yīng)的質(zhì)量管理能力。境外企業(yè)需通過其在中國境內(nèi)設(shè)立的代表機構(gòu)或指定中國境內(nèi)的企業(yè)法人作為代理人。
2. 產(chǎn)品檢驗與臨床評價
* 產(chǎn)品檢驗報告。 產(chǎn)品必須通過具有資質(zhì)的醫(yī)療器械檢驗機構(gòu)進行的注冊檢驗,取得合格的檢驗報告。檢驗項目通常包括性能指標、安全要求(如電氣安全、生物相容性)等。
- 臨床評價路徑選擇。 這是注冊的核心環(huán)節(jié)。對于第二類器械,多數(shù)情況下可通過 “同品種比對” 的路徑進行臨床評價,即通過對比已上市同類產(chǎn)品的臨床數(shù)據(jù),來證明申報產(chǎn)品的安全有效性。若無法進行同品種比對,則可能需要進行臨床試驗。企業(yè)需按照《醫(yī)療器械臨床評價技術(shù)指導(dǎo)原則》等法規(guī)要求,準備詳實的臨床評價資料。
3. 質(zhì)量管理體系核查
* 在注冊申請過程中或受理后,藥品監(jiān)督管理部門會對生產(chǎn)企業(yè)的質(zhì)量管理體系進行現(xiàn)場核查,以確保其具備持續(xù)穩(wěn)定生產(chǎn)合格產(chǎn)品的能力。企業(yè)必須建立并有效運行符合《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》的體系。
4. 技術(shù)審評與行政審批
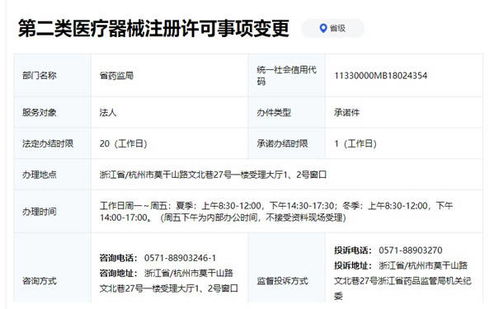
* 將完整的注冊申報資料(包括產(chǎn)品綜述、研究資料、生產(chǎn)制造信息、臨床評價資料、產(chǎn)品風(fēng)險分析、產(chǎn)品技術(shù)要求、說明書標簽等)提交至所在地的省、自治區(qū)、直轄市藥品監(jiān)督管理部門。
- 審評部門對資料進行技術(shù)審評,必要時提出補正意見。審評通過后,由監(jiān)管部門作出準予注冊的行政許可決定,頒發(fā)《醫(yī)療器械注冊證》。注冊證有效期通常為5年。
第二部分:取得注冊證后的銷售關(guān)鍵環(huán)節(jié)
1. 醫(yī)療器械生產(chǎn)許可/備案
* 僅取得注冊證并不意味著可以立即生產(chǎn)銷售。生產(chǎn)企業(yè)還必須向所在地省級藥監(jiān)部門申請 《醫(yī)療器械生產(chǎn)許可證》 (針對生產(chǎn)第二類、第三類醫(yī)療器械)或進行生產(chǎn)備案(針對第一類醫(yī)療器械)。這是對生產(chǎn)資質(zhì)的許可。
2. 經(jīng)營企業(yè)的資質(zhì)要求——醫(yī)療器械經(jīng)營許可/備案
* 銷售方(經(jīng)營企業(yè))必須具備相應(yīng)資質(zhì)。 從事第二類醫(yī)療器械經(jīng)營活動的企業(yè),需向所在地設(shè)區(qū)的市級藥監(jiān)部門提交備案申請,取得 《第二類醫(yī)療器械經(jīng)營備案憑證》。這是合法經(jīng)營的第二類醫(yī)療器械的“入場券”。
- 經(jīng)營企業(yè)需具備與經(jīng)營規(guī)模和范圍相適應(yīng)的經(jīng)營場所、貯存條件、質(zhì)量管理制度和人員等。
3. 上市后監(jiān)管與合規(guī)銷售
* 產(chǎn)品標識與追溯。 銷售的產(chǎn)品必須符合注冊時核準的技術(shù)要求,并附有說明書和標簽。國家推行醫(yī)療器械唯一標識制度,對部分第二類醫(yī)療器械實施UDI管理,以實現(xiàn)產(chǎn)品可追溯。
- 廣告宣傳合規(guī)。 醫(yī)療器械廣告發(fā)布前需經(jīng)省級藥監(jiān)部門審查批準,取得《醫(yī)療器械廣告批準文號》。宣傳內(nèi)容必須真實、合法、科學(xué),不得含有誤導(dǎo)性內(nèi)容。
- 不良事件監(jiān)測與報告。 注冊人和備案人(通常為生產(chǎn)企業(yè))是產(chǎn)品安全責任的主體,必須建立上市后不良事件監(jiān)測體系,及時收集、報告、評價和控制不良事件。經(jīng)營企業(yè)和使用單位也負有協(xié)助報告的義務(wù)。
第三部分:常見風(fēng)險與應(yīng)對建議
- 風(fēng)險一:注冊周期長、成本高。 應(yīng)對:提前規(guī)劃,充分進行法規(guī)調(diào)研和技術(shù)研究,確保注冊資料高質(zhì)量,避免因補正反復(fù)而延誤時間。
- 風(fēng)險二:分類界定不清。 應(yīng)對:在研發(fā)立項早期即咨詢專業(yè)機構(gòu)或向藥監(jiān)部門申請分類界定,明確管理類別和路徑。
- 風(fēng)險三:體系運行與現(xiàn)場核查不符。 應(yīng)對:建立真正有效的質(zhì)量管理體系,并常態(tài)化運行,而非臨時應(yīng)對檢查。
- 風(fēng)險四:銷售環(huán)節(jié)資質(zhì)缺失或管理混亂。 應(yīng)對:經(jīng)營企業(yè)務(wù)必先備案后經(jīng)營,并建立完善的采購、驗收、貯存、銷售、售后服務(wù)管理制度,確保產(chǎn)品來源合法、去向可查。
###
第二類醫(yī)療器械的注冊與銷售是一條嚴謹、專業(yè)的合規(guī)之路。它要求企業(yè)不僅要有過硬的產(chǎn)品研發(fā)和生產(chǎn)能力,更必須具備深刻的法規(guī)理解力和系統(tǒng)的質(zhì)量管理能力。從精準的分類判定開始,到扎實的臨床評價,再到嚴格的體系核查,最終取得注冊證和生產(chǎn)許可,并確保流通環(huán)節(jié)的經(jīng)營者資質(zhì)齊全、管理規(guī)范,每一個環(huán)節(jié)都至關(guān)重要。唯有全程恪守法規(guī),方能確保產(chǎn)品安全有效地服務(wù)于醫(yī)療臨床,同時保障企業(yè)的健康、可持續(xù)發(fā)展。對于計劃進入或已在此領(lǐng)域的企業(yè)而言,持續(xù)關(guān)注法規(guī)動態(tài)、借助專業(yè)力量、構(gòu)建內(nèi)部合規(guī)文化,是應(yīng)對挑戰(zhàn)、把握機遇的不二法門。
如若轉(zhuǎn)載,請注明出處:http://www.baidu0951.com/product/1.html
更新時間:2026-05-09 23:51:00